Vilde Leipart har i sin doktorgrad laget en modell av proteinet vitellogenin og brukt den til å forstå hvordan proteinet fungerer i honningbia. Resultatene er viktige for vår forståelse av honningbia og hvordan vitellogenin påvirker bias helse.
Proteiner er viktige molekylære byggesteiner i levende organismer. De kommer i mange former og størrelser, med en rekke spesialiserte funksjoner.
– Proteiner er ansvarlige for en lang rekke funksjoner, fra muskelbevegelse og oksygentransport, til immunforsvar og genuttrykk, forklarer ph.d.-kandidat Vilde Leipart.
I sin doktorgrad har hun undersøkt proteinet vitellogenin i honningbia. Vitellogenin finnes hos hunkjønnet til mange dyregrupper hos så forskjellige arter som maneter, frosker og høner.
Proteinet bidrar til produksjonen av protein i eggeplomma og er den viktigste kilden til næringsstoffer under tidlig embryoutvikling. Det er nært knyttet til reproduksjon og helse.
Viktig for kubens helse
– Honningbias helse påvirkes av mengden vitellogenin, sier hun.
Proteinnivåene endres etter bienes sosiale oppgaver og påvirker deres forventede levetid. Arbeidere med høye vitellogeninnivåer har for eksempel flere funksjonelle immunceller og bedre motstandskraft mot cellulært stress.
Bedre forståelse for honningbien
Ville og tamme honningbier er både økologisk og økonomisk viktige insekter; de er effektive pollinatorer og produserer honning og bivoks. Arbeidet deres er avgjørende for matsystemene i landbruket, og sikrer overlevelsen til blomstrende planter og dyrene som lever av disse plantene.
– Å sette sammen puslespillet om vitellogeninets betydning for honningbiene er avgjørende for vår forståelse av arten, sier Leipart.
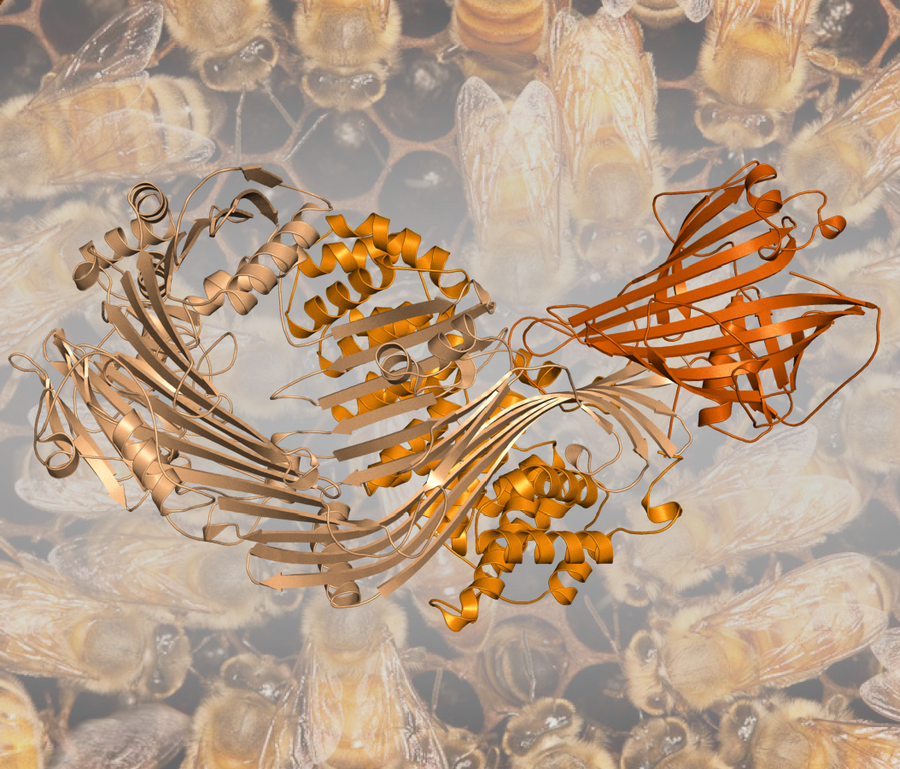
Inngående kunnskap om struktur og funksjon
Leipart har laget en strukturell modell av vitellogenin og brukt modellen til å forstå hvordan proteinet fungerer.
– Strukturen til et protein bestemmer hvordan det fungerer og hva det kan gjøre, forklarer hun.
– Jeg har brukt kunstig intelligens til å forme vitellogeninets struktur. Deretter har jeg testet denne modellen mot et fotavtrykk av det virkelige proteinet hentet fra honningbier.
Leipart har også funnet ut at proteinet kan binde til seg flere ioner av sink. Hun har brukt modellen til å finne disse ionenes potensielle plasseringer.
Høyt genetisk mangfold
Hun har også kartlagt det globale genetiske mangfoldet til vitellogeningenet og skissert de funksjonelle konsekvensene av variasjonen.
– Jeg fant genetiske variasjoner hos individuelle bier ved å samle honningbier fra 15 land, seriekode prøvene og sekvensere hele vitellogenin-genet.
Resultatene hennes viste at genets variasjon er bemerkelsesverdig høy.
Ulike regioner i proteinet, kjent for å ha ulike aktiviteter, som å binde lipidmolekyler eller gjenkjenner sykdomsfremkallende bakterier, viser utpregete variasjoner.
Toppen av isfjellet
Leiparts funn er viktige for å forstå essensielle biologiske prosesser og relevante for de økologiske og økonomisk viktige pollinatorene.
Funnene hennes indikerer at proteinet er svært dynamisk og kan ha flere aktive former. Mekanismen skissert av hennes hypotese er sannsynligvis bare toppen av isfjellet når det gjelder aktivitetene til honningbias vitellogenin.
– Jeg er veldig glad for at jeg fullførte målene mine for prosjektet og var i stand til å utvikle min egen idé om hvordan vitellogenin oppfører seg - på et molekylært nivå.
– Som strukturell biolog er det spennende å presentere et oppdatert syn på proteinets strukturelle landskap. Denne informasjonen er nyttig for mange disipliner og vil bidra til å besvare spørsmål om vitellogenin i mange år fremover.
Vilde Leipart forsvarer sin avhandling "Forståelse av forholdet mellom struktur og funksjon til Vitellogenin i honningbia" fredag 18. februar. Prøveforelesning og forsvar strømmes og er åpne for alle, les mer om det nedenfor.
