Flere «gamle» medisiner som tidligere ble brukt på infeksjoner som malaria, hiv og ebola, er hentet frem som potensielle våpen i kampen mot korona.
På samme måte som et datavirus lurer seg inn i datamaskinen gjennom dens normale innfartskanaler, som e-post eller nedlasting av dataprogrammer, bruker ekte virus samme triks. De lurer seg inn gjennom kroppsåpningene våre.
Når virus har klart å komme seg inn i kroppen vår, bruker de cellenes egne innfartskanaler til å komme seg helt inn i cellenes indre. Ulike typer virus bruker forskjellige strategier til å ta over og kontrollere kroppens egne celler, slik at cellene omgjøres til «virusfabrikker».
Deretter bruker de infiserte cellene det meste av kapasiteten til å tjene sin nye herre – nemlig viruset. Da svekkes cellenes normale funksjoner, samtidig som immunforsvaret vårt prøver å bli kvitt inntrengeren. Til sammen gjør dette at vi føler oss syke.

Viruset som kan føre til sykdommen covid-19, og som har forårsaket pandemien vi er vitne til i disse dager, er et såkalt koronavirus.
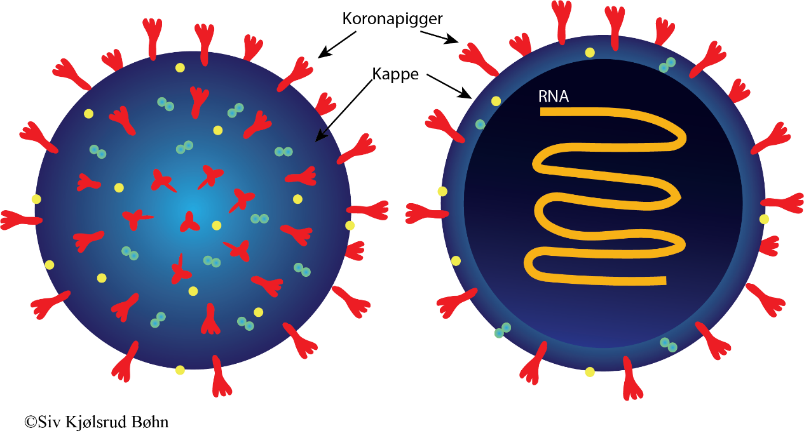
Koronavirus omfatter en stor gruppe av virus som har fått dette navnet på grunn av de spesielle kroneliknende proteinene («koronapigger») på overflaten (se figur 1). Piggene kan også minne om solens corona; den ytterste atmosfæren rundt sola. Når forskerne setter navn på koronavirus skal forkortelsen for «corona» være med i navnet, altså: CoV.
Koronaviruset som nettopp ble oppdaget, og som fører til covid-19, har fått navnet SARS-CoV-2.
Navnet starter med SARS fordi viruset er en variant av SARS-korona-viruset; SARS-CoV, som forårsaket en pandemi av alvorlig lungesykdom i 2003. SARS er en forkortelse for den engelske betegnelsen på sykdommen «Severe Acute Respiratory Syndrome», som på norsk betyr alvorlig akutt respirasjonssyndrom.
Tilstanden er en atypisk lungebetennelse som gjør det vanskelig å puste og hindrer kroppen i å få nok oksygen. I verste fall utvikler sykdommen seg til akutt lungesviktsyndrom (acute respiratory distress syndrome (ARDS) på engelsk).
Inntil SARS-CoV-pandemien i 2003 kjente man til svært få koronavirus som førte til sykdom i mennesker. De fleste koronavirus hadde til da ikke gitt andre problemer enn lette forkjølelsessymptomer.
I 2015 dukket et annet koronavirus opp, nemlig MERS-CoV (MERS= Middle Eastern Respiratory Syndrome Coronavirus), som førte til større dødelighet enn 2003 SARS-CoV.
Figur 1 (artikkelen fortsetter under figuren):
Hvordan kommer viruset seg inn i cellene våre?
For at virus skal gjøre oss syke må de først komme seg inn i kroppen og deretter helt inn i cellene (se figur 2).
Cellene har ikke gjort det lett for virus å komme seg inn. For å få til det, må viruset å ha riktig «nøkkel» til «låsen» på celleoverflaten. Hvis «nøkkelen» ikke passer, vil ikke viruset kunne binde seg til cellens overflate og dermed kommer den seg heller ikke inn i cellen.Fordi de ulike cellene våre har ulike overflateproteiner (= ulike «låser») har virus ofte spesialisert seg på én type celler.
Fordi SARS-CoV-2 er helt nyoppdaget er det mye vi ennå ikke vet om dens egenskaper og hvilke strategier den benytter for å komme seg inn i cellene våre. Siden den deler egenskaper med andre medlemmer av koronavirusene, er det grunn til å mistenke at de vil oppføre seg på omtrent samme måte.
Koronaviruset bruker «korona-piggen» som en «nøkkel» for å låse opp cellen.
En forskningsrapport fra mars 2020 bekrefter at «korona-piggen» på SARS-CoV-2 viruset binder samme overflateprotein som SARS-CoV, viruset som forårsaket en pandemi av alvorlig lungesykdom i 2003.
Dette overflateproteinet, ACE2, finnes det mye av på cellene i luftveiene1. Det forklarer at hoste, tetthet i brystet og kortpustethet hører blant de vanligste symptomene på covid-19. ACE2 sitter også på cellene andre steder, som i tarmen. Derfor kan man også få både magevondt og diarè.
Mengden av ACE2 på overflaten kan være økt hos noen pasientgrupper enten på grunn av sykdommen i seg selv eller på grunn av medisinene de tar. Derfor spekuleres det om dette fører til et høyere opptak av virus i cellene og at dette kan forklare at de fleste som blir alvorlig syke og dør av covid-19 har en "underliggende sykdom". Denne hypotesen er imidlertid ikke testet i noen studier så langt.

Kommer seg inn i cellen via transportveiene
Etter at koronaviruset har klart å binde seg til cellens overflate ved hjelp av «koronapiggen», prøver den å få tilgang til cellens indre. De fleste koronavirus kommer seg inn cellen ved hjelp av transportveien som cellene bruker for å hente inn stoffer de trenger3.
Denne transportveien heter endocytose og foregår ved at blærer med innhold snøres av i overflaten av cellen og tømmes etter de har blitt transportert inn i cellens indre.
Etter hvert kommer viruset seg enda lengre inn i cellens transport- og fordøyelsessystem, og får så tilgang til enzymer som kan kutte av koronapiggene. Dette viser seg å være helt nødvendig for at viruset skal klare å tømme innholdet sitt ut i cellen.
Dersom man på en eller annen måte klarer å stoppe at «koronapiggen» kuttes, har man en potensiell medisin mot viruset.
Arvestoffet til viruset (virus-RNA) vil nå bli kopiert opp i mange kopier ved hjelp av en «kopimaskin» som viruset har fått cellen til å lage. Noen av RNA-kopiene skal brukes som arvestoff i de nye viruspartiklene, mens andre RNA-kopier blir brukt til å infiltrere «proteinfabrikken» til cellen. Cellen vil nå starte med å bruke oppskriften til viruset for å lage virusproteiner i «proteinfabrikken».
Viruset utnytter deretter hele produksjons-, pakke- og transportsystemet til cellen. Dette foregår i spesialiserte avdelinger som heter ER (Endoplasmatisk reticulum) og Golgi-apparatet (se figur 2 under).
I den siste klargjøringsstasjonen i Golgi blir kappen til viruset satt sammen. Denne består av både fett og proteiner. Det neste som skjer er at halvferdige viruspartikler blir en del av cellens eksportsystem hvor de sitter i hulrommene på sammenklemte blærer som beveger seg mot overflaten.
På veien ut vil virus-RNA samle seg i nærheten av viruskappen og etterhvert vil viruset danne et ferdig virus på innsiden av transportblærene. Når transportblærene smelter sammen med overflaten vil viruset slippes ut og den er klar for å komme seg inn i andre celler eller overføres til en ny vert. Hver celle som blir overtatt av et virus har potensiale til å lage tusenvis av viruskopier.
Viruset kan forflytte seg i ørsmå dråper av væske. Man kan få i seg koronavirus ved at man tar seg til øyne, nese eller munn, etter at man har tatt på en overflate hvor viruset sitter.
Hosting og nysing vil føre til at viruset slenges ut og kan smitte videre ved at de pustes inn. Ikke overraskende vil også kyssing være en effektiv smittemåte for viruset.
Figur 2 (artikkelen fortsetter under figuren):

Har vi et antivirusprogram mot koronavirus?
Et antivirusprogram på datamaskinen kan både motvirke virusangrep og fjerne viruset. Har vi et liknende system i kroppen for å beskytte oss mot virus? Svaret på dette er ja. Antivirusprogrammet til kroppen er selvsagt immunforsvaret vårt.
Vi har et medfødt immunforsvar som settes inn umiddelbart etter at viruset har kommet seg inn i kroppen. Deretter vil det adaptive immunforsvaret sette i gang mer effektive antivirus-aktører som til slutt gir oss antistoffproduserende celler og immunitet mot viruset. (Les mer om dette i artikkelen om immunforsvaret av Elin Lunde ved Det Medisinske fakultet, UIO.)
Siden SARS-Cov-2 fra 2019 er cirka 80 prosent genetisk lik varianten fra 2003 og bruker samme «koronapigg» for å binde til ACE2 på cellenes overflate, burde man ikke da være immun mot det nye SARS-Cov-2 hvis man hadde SARS-CoV i 2003?
Dette er jo ganske logisk, men antistoffer som produseres mot 2003-varianten ser ikke ut til å binde SARS-CoV-2 like effektivt. Grunnen til dette er at SARS-CoV-2 er noe annerledes. Blant annet har det en litt annen sammensetning av «koronapiggen».
Selv om den genetiske koden til SARS-CoV-2 ble kartlagt i rekordfart av kinesiske forskere i 2020, antas det at vi mest sannsynlig må vente i minst 18 måneder på at en godkjent vaksine blir allment tilgjengelig, ifølge presseuttalelser fra FHI til NRK i februar 2020.
Virker malaria-, hiv- og ebola-medisiner på SARS-CoV-2?
Mens verden venter på at det skal komme en vaksine mot SARS-CoV-2, finnes det for øyeblikket ingen medisiner eller godkjente vaksiner som kan bekjempe dagens pandemi. Det eneste vi har kunnet gjøre så langt, er å prøve å unngå smitte og la immunforsvaret vårt ordne opp dersom vi blir smittet.
Fordi denne virussykdommen kan bli svært alvorlig med dødelig utfall, jobbes det på spreng for å finne medisiner som kan hindre spredning av viruset og redusere omfanget av sykdommen.
Forskere arbeider nå ut fra flere forskjellige angrepsvinkler.
Flere «gamle» medisiner som tidligere ble brukt på andre infeksjoner, som malaria-parasitten og andre virus som hiv og ebola, er hentet frem som potensielle våpen i kampen mot sykdommen.
Så hvorfor skulle malariamedisin fungere mot virusinfeksjon?
Malariaparasitten benytter samme strategi som koronaviruset for å komme seg inn i cellene. Siden malariamedisin stopper parasitten fra å komme seg inn i cellene og formere seg er det derfor teoretisk mulig at samme medisin kan virke mot koronavirus, men hvordan?
Den klorokin-holdige barken fra det søramerikanske Kinabarktreet var den første medisinen som ble brukt mot malaria. Barken fra treet ble løst opp i vann og den bitre drikken ble drukket for å beskytte mot å bli smittet av sykdommen. Utstasjonerte britiske soldater i India på 1900 tallet forbedret den bitre drikken ved å blande ut barken i sodavann og tilsatte sukker og gin. Dermed var drinken «Gin and Tonic» skapt.
Klorokin, som var den aktive komponenten, virker blant annet ved å hindre malariaparasitten å komme seg inn i blodcellene men den har også andre effekter. Medisinen står på WHO sin liste over essensielle medisiner, og har blitt brukt i over 70 år til å behandle malaria og andre sykdommer som er forårsaket av mikroorganismer, og brukes mot revmatisme, systemisk lupus og Sjøgrens syndrom.
Klorokin kan minske surhetsgraden inne i blærene i cellen. Dette gjør at enzymene som kunne kutte «koronapiggen» ikke virker. På den måten kan klorokinbehandling hindre viruset fra å tømme innholdet sitt inn ut i cellen.
Det er også andre måter klorokin kan bremse viruset på, blant annet at det blir færre ACE2 på overflaten som klarer å binde viruset og den kan hemme kopieringen av virus RNA.
Mange som har tatt klorokin mot malaria har opplevd at de har fått noen ubehagelige bivirkninger. Det er kanskje ikke så overraskende siden klorokin også påvirker cellenes normale opptakssystem. Noen av disse bivirkningene er kvalme, oppkast, hørsels- og synsforstyrrelser, samt lavt blodtrykk.
Nytt liv for «gammel» medisin?
Alle de overnevnte medisinene er eksempler på at «gammel» medisin muligens kan få ny nytteverdi mot noe helt annet enn de opprinnelig ble utviklet for.
Dette har flere fordeler, både vitenskapelige og økonomiske. Det ligger masse forskning bak utviklingen av ethvert legemiddel og det finnes mye informasjon om hvordan legemidler virker, både fra cellestudier, dyrestudier og kliniske studier. Ikke minst har man allerede funnet ut at de ikke gir farlige bivirkninger. Å lage et nytt legemiddel helt fra start er beregnet å ta opptil 12 år og koste så mye som 985 millioner amerikanske dollar.
Selv om medisinene er godkjent for bruk, har de likevel ofte noen mindre farlige bivirkninger. Derfor bør man ikke bruke disse uten at man vet at det virkelig har noe for seg. Dessuten er det «penger ut av vinduet» dersom medisinene ikke virker.
Det kan også hende at medisinene gjør vondt verre for tilstanden man prøver å behandle. Derfor er det nødvendig å teste dette i kliniske studier hvor man sammenlikner en pasientgruppe som har fått medisinen med en annen gruppe pasienter som får vanlig oppfølging uten å få medisinen.
Først etter å ha sammenliknet hvordan det går med disse gruppene vil man kunne si om det virkelig har noe for seg å behandle covid-19 med disse medisinene.

Over hele verden settes det nå i gang studier for å teste ut ulike medikamenter både for behandling og forebygging. Også Norge er i gang med slike studier.
Allerede i mars 2020 ble det igangsatt en klinisk studie ved Oslo Universitetssykehus for å teste ut malariamedisinen hydroksyklorokin, en variant av klorokin som gir færre bivirkninger enn klorokin, og ebolamedisinen remdesivir på pasienter som er innlagt på sykehus for behandling.
Det vil i tiden fremover være viktig å finne ut i hvilke faser av sykdommen det er mest hensiktsmessig å gi disse medisinene. Kanskje vil effekten være avhengig av at man tar medisinen på et tidlig stadium av sykdomsforløpet, men det kan også hende at medisinen har effekt ved langt fremskreden sykdom.
Takk til professor Harald Carlsen (NMBU), og Ronny Bøhn (Msc) for gjennomlesing.
Kilder:
- Ashizawa, N., T. Hashimoto, T. Miyake, T. Shizuku, T. Imaoka and Y. Kinoshita (2006). "Efficacy of camostat mesilate compared with famotidine for treatment of functional dyspepsia: is camostat mesilate effective?" J Gastroenterol Hepatol 21(4): 767-771.
- de Wit, E., F. Feldmann, J. Cronin, R. Jordan, A. Okumura, T. Thomas, D. Scott, T. Cihlar and H. Feldmann (2020). "Prophylactic and therapeutic remdesivir (GS-5734) treatment in the rhesus macaque model of MERS-CoV infection." 117(12): 6771-6776.
- DiMasi, J. A., L. Feldman, A. Seckler and A. Wilson (2010). "Trends in risks associated with new drug development: success rates for investigational drugs." Clin Pharmacol Ther 87(3): 272-277.
- Fang, L., G. Karakiulakis and M. Roth (2020). "Are patients with hypertension and diabetes mellitus at increased risk for COVID-19 infection?" Lancet Respir Med.
- Hamming, I., W. Timens, M. L. Bulthuis, A. T. Lely, G. Navis and H. van Goor (2004). "Tissue distribution of ACE2 protein, the functional receptor for SARS coronavirus. A first step in understanding SARS pathogenesis." J Pathol 203(2): 631-637.
- Kawase, M., K. Shirato, L. van der Hoek, F. Taguchi and S. Matsuyama (2012). "Simultaneous treatment of human bronchial epithelial cells with serine and cysteine protease inhibitors prevents severe acute respiratory syndrome coronavirus entry." J Virol 86(12): 6537-6545.
- Liang, P. H. (2006). "Characterization and inhibition of SARS-coronavirus main protease." Curr Top Med Chem 6(4): 361-376.
- Ou, X., Y. Liu, X. Lei, P. Li, D. Mi, L. Ren, L. Guo, R. Guo, T. Chen, J. Hu, Z. Xiang, Z. Mu, X. Chen, J. Chen, K. Hu, Q. Jin, J. Wang and Z. Qian (2020). "Characterization of spike glycoprotein of SARS-CoV-2 on virus entry and its immune cross-reactivity with SARS-CoV." Nat Commun 11(1): 1620.
- Song, Z., Y. Xu, L. Bao, L. Zhang, P. Yu, Y. Qu, H. Zhu, W. Zhao, Y. Han and C. Qin (2019). "From SARS to MERS, Thrusting Coronaviruses into the Spotlight." Viruses 11(1).
- Vincent, M. J., E. Bergeron, S. Benjannet, B. R. Erickson, P. E. Rollin, T. G. Ksiazek, N. G. Seidah and S. T. Nichol (2005). "Chloroquine is a potent inhibitor of SARS coronavirus infection and spread." Virology Journal 2(1): 69.
- Wouters, O. J., M. McKee and J. Luyten (2020). "Estimated Research and Development Investment Needed to Bring a New Medicine to Market, 2009-2018." Jama 323(9): 844-853.