Utstrakt bruk av kunstgjødsel i jordbruket fører blant annet til utslipp av den potente klimagassen lystgass. Jordbakterier er essensielle i dette; de både produserer og forvandler lystgass!
Helt siden moderne jordbruks spede begynnelse, har vi fremmet plantevekst gjennom tilsetning av nitrogen (N) til jord. I dag resulterer vår generøse distribusjon av kunstgjødsel til økte utslipp av nitrogengass (N₂), dinitrogenoksid/lystgass (N₂O) og nitrogenmonoksid (NO).
Forskningsprosjektet DEPHEND skal øke forståelsen for de mikrobielle prosessene bak disse utslippene.
Jordmikrober er forvaltere av nitrogen
Mikroorganismers stoffskifte driver nitrogenomsetningen og bestemmer utslippsforholdet mellom de respektive nitrogengassene. Utslippsforholdet er viktig, for mens N₂ er harmløs og utgjør nesten 80% av luften vi puster, har utslippene av N₂O og NO alvorlige miljømessige konsekvenser.
Nitrogenmonoksid (NO) er ustabilt og reagerer lett med ulike oksygenformer i troposfæren. Dette resulterer i dannelse av ozon, som er uønsket her. N₂O er, på tross av sitt folkelige navn «lystgass», ikke utpreget festlig i miljøsammenheng. Tvert imot er N₂O den viktigste nedbryteren av stratosfærisk ozon og en drivhusgass nær 310 ganger så potent som CO₂.
Denitrifikasjon – kilde og sluk for N2O
Linda Bergausts forskning går hovedsakelig på å studere fysiologien til prokaryoter, først og fremst bakterier, men også arker, som ved hjelp av et sett med fire enzymer reduserer nitrat og nitritt til N₂ via NO og N₂O. Dette foregår som en respons på at tilgangen til oksygen er begrenset og er en form for anaerob (oksygenfri) respirasjon.
Prosessen kalles denitrifikasjon, og organismer som har denne evnen finnes overalt og i høye antall. I et globalt perspektiv, er denitrifiserende prokaryoter de viktigste produsentene og konsumentene av N₂O i jord.
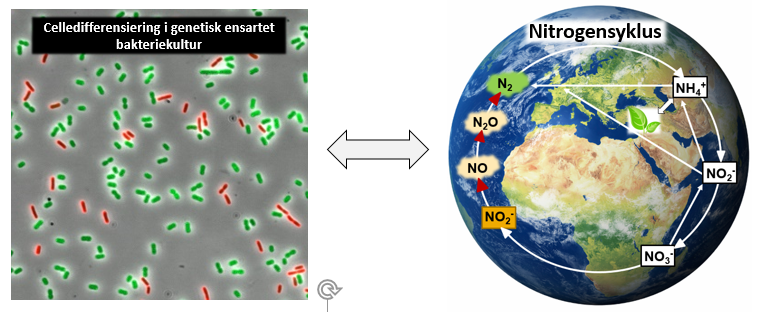
Varierende tilgang på oksygen skaper utfordringer
Denitrifiserende bakterier foretrekker oksygen for respirasjon, men om det skjer endringer i tilgangen på oksygen, for eksempel når jorden mettes med vann, må de bestemme seg for hvilke investeringer de skal gjøre med de oftest fattigslige energireservene de har.
Hvis tilgangen på oksygen minker eller stopper opp, kan organismene bruke nitrogenoksider (nitrat, nitritt, NO, N2O) i stedet for oksygen til respirasjon, slik at de konserverer energi i form av dannelse av adenosin trifosfat (ATP). ATP er cellenes energivaluta og er en slags universell energileverandør i alle celler og vev.
For å kunne bruke de nevnte nitrogenforbindelsene må imidlertid organismene ha det enzymatiske apparatet på plass og det må de danne før oksygenet er helt borte. Dette kalles å syntetisere enzymer – og er en energikrevende «investering» som på kort sikt kan gå på bekostning av vekst for organismen.
Prokaryotenes energiøkonomiske dilemma
Skal jordbakteriene «tro» at de nye, oksygenfattige forholdene varer en stund, syntetisere alle enzymene de trenger for å redusere nitrat hele veien til N2 og på den måten sørge for høyest mulige anaerobe (oksygenfrie) vekstrate og -utbytte? Eller skal de holde tilbake og nøye seg med å syntetisere kun deler av denitrifikasjonsapparatet, med de følger det har for veksthastigheten så lenge oksygen er utilgjengelig?
Om de står foran en langvarig oksygenfattig periode er full investering i denitrifikasjon en god idé, men dersom oksygenet raskt kommer tilbake, har de kastet bort verdifull energi på å bygge et maskineri de ikke lenger trenger.
Om de derimot kun har investert et minimum for å sikre overlevelse under korte oksygenfattige perioder, har de en fordel i tilfeller der oksygen raskt vender tilbake. Dermed kan man si at når oksygenet forsvinner, må bakteriene inngå et veddemål: kommer oksygenet raskt tilbake, eller blir endringen langvarig?
Gamblende bakterier og N₂O sluk
Enkelte jordbakterier oppfører seg nettopp i tråd med dette. Når de oppdager at oksygen er i ferd med å forsvinne, syntetiserer alle celler i en kultur enzymet som reduserer N2O til N2. Samtidig er det kun et fåtall som investerer i resten av denitrifikasjonsenzymene. I starten av en oksygenfattig fase vil dermed noen celler vokse fort og både produsere og redusere N2O, mens flertallet av celler vil vokse sakte og basert på reduksjon av små mengder N2O frigitt fra mindretallet. Vi sier at det har skjedd en celledifferensiering og slike kulturer blir nettosluk for N2O under forhold der oksygentilgangen svinger raskt.
På grunnplanet
DEPHEND er i høy grad et grunnforskningsprosjekt og veien frem til faktisk implementering av oppdagelser er lang. Samtidig vil arbeidet foregå i en kontekst hvor funn raskt kan tas videre og testes i mer komplekse systemer.
Prosjektet vil kombinere molekylære metoder, mikroskopiteknikker, detaljerte studier av gasskinetikk i renkulturer og matematisk modellering. Målsetningen blir å oppnå en større forståelse for mekanismene bak celledifferensiering i denitrifiserende bakterier, utbredelse og implikasjoner for utslipp av NO og N₂O fra jord til atmosfære.
Fakta
FRIPRO-prosjektet DEPHEND starter opp i 2018 med midler fra Forskningsrådet gjennom FRIPRO/FRIMEDBIO
Prosjektet bygger på oppdagelsen av såkalt fenotypisk plastisitet eller celledifferensiering hos enkelte denitrifiserende bakterier.
Arbeidet vil foregå som et samarbeid mellom Linda Bergaust og kolleger ved KBM/NMBU, og partnere ved Universitetet i East Anglia (UK) og Universitetet i Vrije (NL).
Varighet: 3,5 år
Ramme: 8 millioner kroner
